回望2025年,醫學領域迎來了一個激動人心的突破之年。
那些曾存在于理論中的前沿科技,正以前所未有的速度走進現實:致命的遺傳病看到了被根治的曙光,帕金森等慢性病實現了癥狀的顯著逆轉,部分患者得以告別終身服藥,癌癥患者的生存期也在不斷延長……這些里程碑的背后,是無數科研與臨床工作者經年累月的探索,讓一篇篇深奧的論文,最終化作拯救生命的新療法。
在這辭舊迎新之際,我國“醫學界”編輯部延續傳統,精心遴選出?“2025年度十大臨床突破”?。從中可以清晰看到,中國在醫療創新領域成果顯著,尤其在細胞與基因治療、再生醫學等前沿方向,已逐步走在世界前列。

接下來,就讓我們一起走近2025年醫學界的十大臨床突破,看看它們究竟帶來了哪些改變,又將如何影響未來的醫學發展與患者生活。
以下為“十大臨床突破”(按時間順序):
- 中國醫生將基因編輯豬肝植入人體
- 腫瘤疫苗硬剛“癌癥之王”
- 定制基因編輯療法治療嬰兒遺傳病
- 干細胞療法成功治療帕金森病
- 長效降脂的新時代
- 無須免疫抑制的胰島移植治療1型糖尿病
- 全球唯一可降解房間隔缺損封堵器
- CAR-NK療法治療紅斑狼瘡
- 中國團隊破解“外科打結”難題
- 皰疹疫苗提供全方位保護
2025年全球十大臨床突破揭曉:3項細胞療法上榜,聚焦帕金森、1型糖尿病與紅斑狼瘡治療
01.中國醫生將基因編輯豬肝植入人體
2025年1月7日,空軍軍醫大學西京醫院竇科峰院士團隊完成全球首例“原位豬全肝”人體移植:將一只經過基因編輯的豬肝,原位植入一名腦死亡患者體內。手術恢復血流后,豬肝迅速開始分泌膽汁,并承擔起正常肝臟的生理功能,驗證了其在人體內工作的可行性。[1]

這是全球首次實現豬肝在人體內的原位替代,為豬肝作為急性肝衰竭“過渡治療”提供了關鍵醫學證據,受到國際學界高度關注。此前,全球20余例異種器官移植主要集中在心臟和腎臟領域,中美處于領先位置,而此次突破填補了肝臟領域的空白。
與此同時,異種移植的生存紀錄不斷刷新。2025年,美國團隊創造了豬腎在人體內工作271天的全球最長紀錄;隨后,西京醫院完成的亞洲首例異種腎移植患者生存261天,位居全球第二。
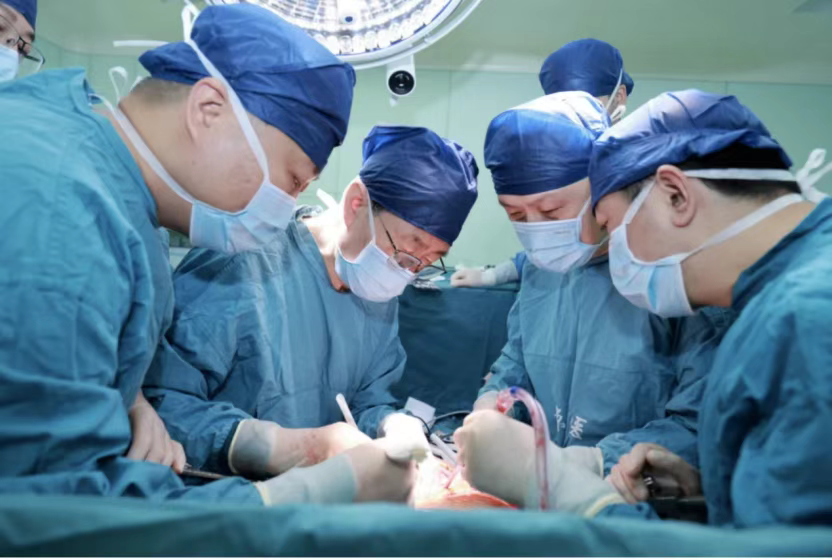
器官短缺是移植醫學的核心難題——全球每年約有200萬人需要器官移植,但不到10%能等到合適器官。學界普遍認為,經過基因編輯的豬器官有望成為可規模化供應的替代來源。
隨著2025年11月美國啟動首例豬腎人體移植臨床試驗,異種器官移植正從“特殊救治”邁向規范化臨床應用。有專家預測,未來5年內,豬腎移植有望成為常規手術之一。
02.18個月無復發,腫瘤疫苗硬剛“癌癥之王”
2025年2月,《自然》雜志發表了一項關于個體化mRNA腫瘤疫苗BNT122的重要研究。該疫苗旨在降低胰腺導管腺癌(PDAC)患者手術后的復發風險。[2]
胰腺癌被稱為“癌癥之王”,其中PDAC占大多數,即使成功手術,超過60%的患者也常在一年內復發,5年生存率不足10%。
BNT122是一種為患者量身定制的疫苗。治療時先對腫瘤樣本進行基因測序,找出癌細胞的特有突變,據此設計并合成mRNA疫苗,以此激活患者自身的免疫系統精準攻擊腫瘤。
研究顯示,8名產生免疫應答的術后患者,在18個月內均未復發。隨訪3.2年時,其中6人仍無復發跡象,且中位無復發生存期尚未達到。疫苗激發的T細胞免疫應答強勁,部分T細胞可能存活超過10年,提示其具有長期保護潛力。
不僅是BNT122,2025年以來,全球多款mRNA腫瘤疫苗研發進展迅速,在胰腺癌、卵巢癌等以往難以應對的“冷腫瘤”中展現出新的治療希望。
03.定制基因編輯療法治療嬰兒遺傳病
2025年2月25日,全球首個為個體定制的體內堿基編輯療法成功應用于臨床,挽救了一名6個月大男嬰的生命。這項發表于《新英格蘭醫學雜志》的案例,為罕見遺傳病的精準治療開辟了新路徑。[3]

該嬰兒患有罕見的“CPS1缺乏癥”,傳統治療需嚴格限制飲食或進行肝移植,嬰兒期死亡率高達50%。一支多國科學家團隊迅速響應,在短短6個月內,專門為他開發出一款堿基編輯療法,精準修復致病基因,創造了基因療法從研發到應用的最快紀錄。
此次治療展示了在緊迫臨床需求下,國際科研團隊高效協作、將前沿技術快速轉化為救命方案的強大能力。盡管該技術要廣泛應用仍面臨編輯效率、持久性及成本等挑戰,但它首次驗證了為危重遺傳病快速開發定制化基因療法的可行性。
目前,美國已啟動新的研究項目,旨在將此類精準治療從“拯救一個嬰兒”推廣到“挽救成千上萬的孩子”。
04.干細胞療法成功治療帕金森病
2025年4月16日,《自然》發布日本京都大學醫院團隊“干細胞治療帕金森病”的兩年隨訪結果,6名患者中有4人停藥期的運動功能改善,5人用藥期間改善,均未出現嚴重的不良事件。[4]
這是全球首次在臨床中嘗試使用基于誘導多能干細胞(iPSC)的細胞移植療法治療帕金森病。

據統計,全球約800萬帕金森病患者目前無法被根治,傳統藥物僅能緩解癥狀而無法阻止病情惡化。干細胞療法則提供了新的可能。該療法基于2006年諾貝爾獎得主山中伸彌教授開創的iPSC技術,這類細胞能無限增殖并分化為包括關鍵的多巴胺能神經元在內的各類細胞,從而有望從根源上修復神經損傷。
在我國,相關臨床探索也已取得實質性進展。今年4月初,上海瑞金醫院劉軍教授團隊通過類似技術路徑,在臨床試驗中使一名病程長達14年的帕金森病患者出現明顯運動功能恢復。10月,安徽省立醫院副院長施炯教授團隊完成治療,全球首例被報道為實現“功能性治愈”的早發型帕金森病(EOPD)患者由此誕生。
放眼全球,干細胞治療帕金森病的研究正在加速推進,已有十余項相關臨床試驗同步開展。同時,干細胞療法也被拓展至糖尿病、眼科疾病、心力衰竭等多個領域。隨著臨床證據不斷積累,這些長期被視為不可逆的疾病,或許正迎來被重新定義的治療可能。
05.長效降脂新時代
2025年7月31日,美國FDA批準了長效降脂藥英克司蘭(Inclisiran)拓展新適應證,允許其作為單一療法,每年注射兩次即可用于降低血脂。這為高脂血癥患者提供了無需每日服藥的新選擇。[5]

我國心血管病患者超3億,防治形勢嚴峻。長期以來,每日口服他汀類藥物是控制血脂、預防心血管事件的基石療法。英克司蘭則是一種小干擾RNA藥物,通過“基因沉默”機制長效降低“壞膽固醇”,此前獲批時需與他汀聯用。
今年5月公布的關鍵III期研究顯示,英克司蘭單藥降脂效果與他汀相當,從而直接推動了此次適應證變更。這意味著符合條件的患者可實現從“每日服藥”到“一年兩針”的轉變,有望顯著提高治療依從性,并可能影響全球治療指南。
當然,該藥單用對心血管結局的長期影響仍有待最終數據證實,且其年治療費用遠高于他汀,目前可及性有限。盡管如此,英克司蘭仍標志著一個重要趨勢:以核酸藥物為代表的“長效甚至一次性”慢性病治療模式,正在逐步走向現實。
06.無須免疫抑制的胰島細胞移植治療1型糖尿病
2025年8月4日,瑞典烏普薩拉大學等機構研究人員在《新英格蘭醫學雜志》(NEJM)發表重磅研究,全球首次通過基因編輯改造的異體胰島β細胞,在不使用免疫抑制劑的情況下,成功治療了一名病史長達37年的1型糖尿病患者。[6]

全球約有920萬1型糖尿病患者,傳統上,移植從捐獻者胰腺中提取的胰島組織是潛在的“治愈”手段,但移植后患者需終身使用具有毒副作用的免疫抑制劑來對抗排斥反應。
這項名為UP421的新療法則通過基因編輯,敲除了供體胰島細胞中引發免疫排斥的關鍵基因,并增強了其免疫逃逸能力,從細胞本源上解決了排斥問題。
治療后的數據顯示,即便在不使用任何免疫抑制劑的情況下,移植的“新胰島”在患者體內成功存活并持續分泌胰島素,這一效果至少維持了半年。這標志著,幾十年來器官移植領域追求的“免疫耐受”目標取得了關鍵進展。
這項研究的深遠意義在于,它將移植的免疫挑戰從術后的“長期管理問題”,前移至細胞制備時的“工程化設計問題”。未來的競爭核心不再是簡單的細胞移植,而是能否通過可驗證、可迭代的基因工程模塊,一勞永逸地解決免疫排斥。
該療法已計劃推進更大規模的臨床試驗,其最終目標是讓患者無需終身醫療干預,即可實現穩定的血糖控制。正如專家所言,糖尿病治療的“范式轉變”已經到來。
07.全球唯一可降解的房間隔缺損封堵器
2025年10月23日,我國團隊在《美國醫學會雜志》(JAMA)上發表了全球首款生物可降解房間隔缺損(ASD)封堵器的臨床應用研究。該器械不僅能在植入后安全有效地閉合心臟缺損,還能在兩年內完全降解,并促進自身組織再生。[7]

房間隔缺損是一種常見的先天性心臟病。過去二十多年,微創介入植入金屬封堵器是標準療法,但患者體內會永久留有異物,可能帶來遠期并發癥。
讓封堵器在完成使命后自然降解,是全球該領域的追求目標。我國科學家成功攻克了可降解材料在術中顯影等技術難題,結合創新的“無輻射”介入技術,實現了可降解封堵器的精準植入。
這項研究是JAMA創刊近150年來首次刊登中國原創醫療器械的臨床研究,標志著我國在高端醫療裝備領域,已完整掌握了從材料研發、器械制造到臨床驗證的全鏈條創新能力。國際評審專家評價,這是該領域近三十年來“最具里程碑意義的突破”。
08.治療紅斑狼瘡,CAR-NK療法破局
2025年11月13日,上海長海醫院風濕免疫科團隊在《柳葉刀》(The Lancet)發表重磅研究,全球首次系統性報道CAR-NK(嵌合抗原受體NK細胞)療法用于治療難治性系統性紅斑狼瘡(SLE),并取得令人矚目的臨床效果。[8]

目前,全球約有800萬名SLE患者。該病可累及多器官系統,導致長期疲勞、皮疹、關節疼痛,嚴重者甚至危及生命。盡管 CAR-T療法曾讓人們首次看到治愈SLE的可能,但其高昂費用以及細胞因子風暴、嚴重感染等安全風險,限制了在自身免疫病中的廣泛應用。
長海醫院趙東寶、高潔團隊將目光轉向CAR-NK療法。該技術可直接清除體內致病的漿細胞,雖然殺傷強度相對CAR-T更為溫和,但安全性更可控,同時具備“現貨型”生產潛力,理論上可將治療成本降至自體CAR-T的十分之一。
研究結果顯示,治療后6個月內所有患者病情均得到控制:
- 13名患者維持低疾病活動狀態
- 10名患者實現完全臨床緩解
在隨訪超過1年的9名患者中,6人保持完全緩解或疾病低活動度,且無一例復發。

《柳葉刀》隨刊評論指出:“這標志著 CAR 細胞療法在自身免疫病轉化研究中邁出了關鍵一步。”
其臨床意義已經十分清晰:隨著細胞療法的發展,SLE等自身免疫病實現長期緩解乃至治愈,正逐步從設想走向現實。
09.中國院士團隊破解“外科打結”難題
2025年11月27日,浙江大學楊衛院士與蔡秀軍院士的跨學科團隊在《自然》雜志發表封面論文,創新性地提出并應用了“Sliputure”——一種能自動感知并鎖定最佳張力的活結智能縫線,成功解決了外科縫合中長期存在的張力控制難題。[9]

在外科手術中,打結的松緊度至關重要:過松可能導致傷口裂開,過緊則可能阻礙局部供血,造成組織損傷。傳統外科結一旦打牢便無法調整。
研究團隊獨辟蹊徑,沒有依賴復雜的電子傳感系統,而是回歸力學本質,通過材料學、醫學、數學與機械工程的深度交叉,設計出這種特殊的縫線。其核心是一個巧妙的“活結”結構:當外科醫生或機器人拉緊縫線時,活結會在達到理想張力的瞬間自動解開,并轉化為一個牢固的“死結”,精準鎖定最佳力度。
實驗顯示,使用該技術能讓經驗不足的年輕醫生將縫合精確度提升121%,達到資深專家水平。《自然》雜志以封面形式報道了這項“四兩撥千斤”式的創新,它用簡潔而智慧的跨學科方法,成功攻克了一個長期困擾外科臨床的精細操作難題。
10.皰疹疫苗提供全方位保護
2025年12月11日,《細胞》發布帶狀皰疹疫苗重磅研究成果,表明其能顯著降低輕度認知障礙的發生風險,減緩疾病進程,降低癡呆導致的死亡風險。今年早些時候,《自然》《美國醫學會雜志》《自然·醫學》等也發布了類似結果。

此外,5月《歐洲心臟雜志》、2025年歐洲心臟病學會年會的研究,則全面評估皰疹疫苗接種與心血管事件的關聯。其中一項百萬人分析表明,接種皰疹疫苗能使心血管病總體風險降低23%,保護效果可持續8年之久。
這些突破性發現將慢性病預防的思路引向了一個充滿潛力的新方向——“感染與免疫”干預。隨著人口老齡化,我國面臨沉重的癡呆與心血管疾病負擔,同時50歲以上人群帶狀皰疹年新發超150萬例。如果其多重保護效果得到最終確認,這意味著通過接種一種安全性已知的疫苗,可能為數億面臨相關疾病風險的成年人,提供一條兼具成本效益的預防新路徑。
結語
2025年的這些突破,不僅彰顯了醫學研究與臨床實踐的驚人速度,也讓曾被視為不可逆的疾病、難治的病癥迎來了新的可能。每一項進展,背后都是科學家們日復一日的探索與創新,是技術、臨床與患者需求的完美結合。
展望未來,隨著基因編輯、干細胞、個性化疫苗和智能醫療器械等前沿技術不斷成熟,我們有理由相信,更多“無法治愈”的疾病將被重新定義,更多患者將享受到精準、安全、可持續的治療方案。醫學的邊界正在被不斷拓展,2026年,新的希望與突破也必將接踵而至。
參考資料:
[1]https://www.nature.com/articles/s41586-025-08799-1
[2]Sethna, Z., Guasp, P., Reiche, C.?et al.?RNA neoantigen vaccines prime long-lived CD8+?T cells in pancreatic cancer.?Nature?639, 1042–1051 (2025). https://doi.org/10.1038/s41586-024-08508-4
[3]https://www.nejm.org/doi/abs/10.1056/NEJMoa2504747#tab-citations
[4]Sawamoto, N., Doi, D., Nakanishi, E.?et al.?Phase I/II trial of iPS-cell-derived dopaminergic cells for Parkinson’s disease.?Nature?641, 971–977 (2025). https://doi.org/10.1038/s41586-025-08700-0
[5]https://www.novartis.com/us-en/news/media-releases/novartis-twice-yearly-leqvio-inclisiran-receives-fda-approval-new-indication-enabling-first-line-use
[6]https://www.nejm.org/doi/full/10.1056/NEJMoa2503822
[7]Ouyang W,?Jiang H,?Yan X, et al. Bioresorbable vs Metallic Occluders for Transcatheter Atrial Septal Defect Closure:?A Randomized Clinical Trial.?JAMA.?2025;334(19):1740–1749. doi:10.1001/jama.2025.17639
[8]https://www.thelancet.com/article/S0140-6736(25)01671-X/abstract
[9]https://www.chinanews.com.cn/jk/2025/11-27/10522322.shtml?utm_source=chatgpt.com
[10]The effect of shingles vaccination at different stages of the dementia disease courseXie, Min et al.Cell, Volume 188, Issue 25, 7049 – 7064.e20
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。




 掃碼添加官方微信
掃碼添加官方微信